
随着医学影像分析技术的快速发展和临床影像数据量的急剧增长,如何快速准确针对不同疾病医学影像进行精确诊断、分类和预后评估,是现代医学工作者面临的重大挑战。深度学习是一种高通量自动化提取高维度特征信息的新一代人工智能技术,目前已广泛应用于临床医学大数据分析领域,为临床医学影像的快速识别、精准分割和辅助诊断等分析工作提供了新的机遇。下文搜集了一些材料,将全面介绍一下近年来深度学习技术在医学影像分析领域的研究情况,探讨在MRI(核磁共振)、CT、超声和X线等医学影像分析中的重要方法和典型应用,供各位读者学习了解。
1998年科学家首次提出了神经网络雏形LeNet,利用反向传播算法训练多层神经网络为深度学习奠定了基础。在此之后涌现出更多优秀的深度学习算法,如2012年ImageNet图像分类竞赛冠军AlexNet,2014年ILSVRC定位任务第一名和分类任务第二名的VGGNet,这些算法在医学影像分类、定位、分割和重建方面均取得了较好的效果。
新一代非监督深度学习网络如PixelRNN/卷积神经网络、变分自编码器、生成式对抗网络和多层降噪自动编码机等无需使用带标签的数据训练,能解决影像训练样本不足的问题,并节省了人工标记影像感兴趣区域的步骤。近年发展较快的深度强化学习具有自动学习的功能,能够根据反馈不断调整自己的输出以达到最优结果。其他深度学习网络模型如循环神经网络在具有不同特点的医学影像分析问题中取得了较好的效果。
由于医学影像存在着对比度低、可变性大和结构复杂等特点,目前尚无一种通用的方法来解决不同成像方式和不同疾病的辅助诊断,下文按照不同成像方式对现有的深度学习方法应用进行了梳理,列举了近年来深度学习方法在不同医学场景的应用。总结表明,将传统的深度学习方法与实际图像特点相结合的改进方法能够有效适应医学图像的特征,将是医学辅助诊断发展的重要趋势。
01 深度学习在MRI影像分析中的应用
MRI可获得反映不同人体组织器官特性的影像数据,是临床影像检查中的常用方法。由于不同序列MRI影像中信息量较大,一些组织器官的信号相近,临床上依赖有一定工作经验的影像科医生进行看片解读。近年来,针对MRI影像的计算机辅助分析技术能够快速准确批量处理影像数据,在对不同疾病进行准确诊断、精准分割、分类和预后等方面显示出巨大的应用潜力,得到医学影像工作者的高度关注。
当前用于MRI影像分析的深度学习方法主要有三类:基于小块图像组的Patch-Wise CNN模型,基于语义的Semantic-Wise CNN模型和基于级联网络的Cascade CNN模型。
基于小块图像组的Patch-Wise CNN模型结构具有收敛速度快的特点,在医学图像诊断和分割领域中已有广泛应用。Ghafoorian等使用Patch-Wise CNN尝试分割白质高信号区域,网络获得的分割结果与医生手工分割图像没有统计学差异。Moeskops等采用了不同尺寸的2D图像组作为输入,并使用了不同大小的卷积核,获得分割图像Dice相似系数值范围为0.82~0.91,并表明小尺寸图像组训练的网络可以对微小组织结构进行精细分析。Kamnitsas等设计了含有双通路的3D卷积网络DeepMedic模型,使用条件随机作为后处理,在TBI、BRATS 2015和ISLES-SISS 2015数据库中测试的DSC值分别达到了63.0、89.8和66.0。这些研究均表明Patch-Wise CNN框架在MRI影像的分割中具有重要的研究价值和应用潜力。
与Patch-Wise CNN模型只能将固定尺寸的影像输入网络不同,基于语义的Semantic-Wise CNN模型先通过卷积获得图像的高层次特征,再通过去卷积输出分割图像,从而能够将任意大小的影像作为输入,且具有更少的网络参数,训练所需的耗时更短。Jonathan等最早基于语义分割思想提出了端对端的全卷积网络概念,对整幅输入影像进行卷积处理,学习高维度抽象信息,再通过去卷积处理获得对不同种像素的分割输出。Brosch等将FCN网络框架用于多发性硬化病灶MRI影像的分割研究,虽然分割使用的数据集较小,仍获得了68.4的DSC值。Nile等进一步采用使用该网络框架对人体正常组织的MRI影像进行了分割,并测试了单模态和多模态输入对网络的影响,表明模型泵从多模态输入中获取更丰富的高维度信息。
基于级联网络的Cascade CNN模型是将一个CNN的输出作为另一个CNN的输入,第一个CNN用来勾画组织器官的大体区域,第二个CNN则用来进行精细分割,判断每个像素是否属于该组织器官,这可以使得整个网络更加高效,且所需影像的训练样本较少。该网络的主要特点是在第二轮计算中只针对筛选出的感兴趣区进行分析,可以显著减少冗余计算,不仅能区分正常组织和病变区域,而且在病变区域内部还可以进一步实现细分类。Valverde等利用Cascade CNN网络对多发性硬化症MRI影像进行了分割,结果表明Cascade CNN网络可以在保持假阳性率较低的基础上大幅提高分割精确度。Cui等也使用Cascade CNN对脑胶质瘤MRI影像进行了分割,他们采用FCN网络结合迁移学习的方法先挑选出影像中的肿瘤区域,再使用深层CNN网络结合小卷积核进一步对肿瘤影像进行精确分割,该方法在BRATS2015公开MRI影像数据集上的DSC值可达0.89,计算耗时仅需1.54s。表1为近年来提出的一些有代表性的用于脑部MRI影像分割的重要深度学习模型。

02 深度学习在CT影像分析中的应用
针对CT影像的计算机辅助分析技术的研究时间最长,且技术发展较为成熟。已有大量研究表明,利用深度学习对多层CT影像进行筛选和分类的辅助诊断技术能为临床医生提供有价值的参考意见。对CT影像进行适当的预处理可以有效提高深度学习模型对肺结节的分类能力,Ciompi等通过将肺部CT影像垂直的横切面、矢状面和冠状面进行旋转扩充,获得不同切面的结节图像,从而解决了临床训练数据不足的问题。Shen等模拟医生阅片时的远观和近看过程,对同一结节图像进行了缩放处理后再进入深度学习网络,模型的分类效果获得了显著提高。此外,近年的研究发现,使用自然图像对神经网络进行预先训练后,再利用肺CT影像对模型二次训练,可以显著提高结节的分类效果。Ciompi等使用ImageNet数据库预先训练好的网络,并通过微调使其更加适用于肺结节的分类任务。Hoo-Chang等也利用ImageNet对AlexNet和GoogLeNet分别进行训练和微调,分类效果也得到了明显提升。Erhan等则进一步采用无监督预训练联合监督式微调进行训练,提高了对肺结节的分类能力。
多种网络模型融合策略也常用于肺部CT影像中结节分类鉴定。Zhao等将LeNet和AlexNet进行融合后,分类准确率为82.25%,AUC值达到87.70%。Shen等提出含有特殊池化层结构的Multi-Crop CNN模型,能将卷积层输出的中心特征提取出来,再将多个Multi-Crop提取的特征进行集合后再继续卷积操作,该模型的分类准确度为87.14%,AUC值高达0.93。Ali等在现有CNN网络模型的基础上,进一步提出了强化学模型,并在LIDC-IDRI数据集上进行了测试,结果表明RL模型在训练集中能得到很高的准确率和敏感度,但在测试集上却较低,这可能是由于RL模型对数据量的需求较大,对于大于3mm的结节,单个放射科医师的错误发现率为65.2%,而RL模型的为44.7%,体现了强化学习策略在CT影像分析中的优势。
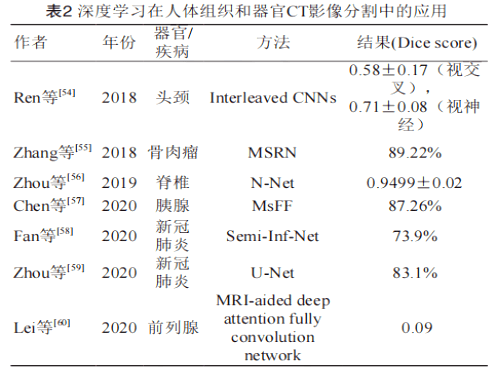
在术前定位及放疗定位中,病灶轮廓勾画的不精确会对放疗计划的剂量学特性产生巨大影响及对正常组织造成毒性损伤,因此基于CT影像的器官轮廓精准分割有着重要的临床价值,而现有分割方法多采用手动分割,存在人为误差。近年来,深度学习技术在CT影像分割领域取得了一系列重要研究进展。在腹部CT影像分割领域,由于腹部器官较多且CT值相近,因此精准分割各器官轮廓是非常困难的。
参考文献《深度学习人工智能技术在医学影像辅助分析中的应用》
